8) Was beweisen die Fakten zur Entstehung des Lebens?
(Fortsetzung meines Briefes vom 23.8.1994.)
(Prof. C.:) "Schließlich ist auch die Bemerkung von Conklin (S. 598) zur Wahrscheinlichkeit der Entstehung des Lebens "durch Zufall" heute längst durch die Thesen von Nobelpreisträger M. Eigen, P. Schuster und anderen widerlegt. "
(W.-E.L.:) Nachdem ich mich einige Jahre lang gründlich mit dieser Frage beschäftigt habe, bin ich zu dem Ergebnis gekommen, dass nicht Conklins Überlegungen, sondern Eigens Thesen längst widerlegt sind, und zwar insbesondere durch die Tatsache, dass die von Eigen u. a. angenommenen "Ursuppen" -und das ist seit Jahrzehnten bekannt und entspricht auch dem neuesten Stand der Wissenschaft -wahrscheinlich niemals existiert haben. Damit fehlt die naturwissenschaftliche Grundlage für alle weiteren Schlussfolgerungen von den postulierten einfachen präbiotischen Syntheseschritten bis hin zu den Hyperzyklen.
Eigens Voraussetzungen sind u. a. durch den bekannten Polymerchemiker Prof. B. Vollmert widerlegt worden. Seit etwa 1985 unterlässt es Eigen jedoch, Vollmert in seinen Arbeiten zu zitieren und zu widerlegen. Eine solche Methode, den wissenschaftlichen Gegner zu ignorieren, kann nicht dem wissenschaftlichen Fortschritt dienen. Eigen diskutiert nicht mehr das zur Wahrheitsfindung grundlegende wissenschaftliche Für und Wider seiner Hypothesen (Wahrscheinlichkeit der "Ursuppe", Bildung von biologisch relevanten Polymeren etc., vgl. die unten wiedergegebenen Argumente), sondern verkündet ex cathedra mit der Autorität des Nobelpreisträgers die grundsätzliche Richtigkeit seiner Anschauungen. Mit Erfolg, ist hier hinzuzufügen, - aber ich vermute, dass auf die Dauer mit einer solchen Methodik das Ansehen der Naturwissenschaft in Mitleidenschaft gezogen wird (spätestens wenn der Öffentlichkeit klar wird, dass es sich hier um ein evolutionäres Luftschloss statt um historische Realitäten gehandelt hat).
Dazu einige Daten aus den Arbeiten mehrerer evolutionistischer Autoren, zitiert nach Hans Krause 1986 (Das Leben auf der Erde: Die erste Zelle - wie entstanden? Stuttgart) (N.: Herr H. Krause hat diese Arbeit im Jahre 1999 auf den neusten Stand gebracht; siehe:
Die Zelle: Ihre Ursache 1, Die Zelle: Ihre Ursache 2 und Das Leben auf der Erde. Die erste Zelle - Wie entstanden? . - Da ich dem Leser jedoch einen möglichst vollständigen Einblick in die seinerzeit geführte Diskussion zwischen Herrn C., D. und mir geben möchte, halte ich mich hier an die damals übersandten Texte. Die folgenden Argumente sind übrigens nach wie vor stichhaltig!)Hans Krause schreibt 1986, pp. 76-90:
"Die erste Zelle, so meint Professor Manfred Eigen, habe sich von selbst in einer "Ursuppe entwickelt, die "so gehaltvoll" gewesen sei, "wie eine kräftige Fleischbrühe" (1981) S. 39, 40.
METHAN-AM MONIAK -WASSERSTOFF-REICHE
URATMOSPHÄRE
Nach der Hypothese von der chemischen Evolution soll sich die erste Zelle auf der Erde von selbst nur durch die Naturgesetze aus lebloser Materie entwickelt haben, weil die Atmosphäre des frühen Präkambriums stark reduzierend war und viel Methan, Ammoniak und freien Wasserstoff enthielt. In dieser reduzierenden methan-ammonium-wasserstoff-reichen Uratmosphäre sollen sich die Bausteine des Lebens durch Zufall gebildet haben und dann auf die Oberfläche der Erde und des Meeres herabgerieselt sein. Im Urmeer sollen sich die Aminosäuren dann in Hunderten von Millionen, wenn nicht in Milliarden von Jahren zu einer dicken chemischen Suppe angesammelt haben, so dick, wie eine kräftige Fleischbrühe. Einige Anhänger von Professor A. I. Oparin sind zu dem Schluss gekommen, dass die Bausteine des Lebens nicht in der Uratmosphäre entstanden sein können, weil die starke ultraviolette Strahlung sie zerstört hätte. Sie glauben statt dessen, dass die Bausteine des Lebens nicht aus den Chemikalien der methan-ammoniak-reichen Uratmosphäre gebildet worden seien, sondern im Meer, weil sich die nötigen Chemikalien im Meer erhalten und sich anreichern konnten.
Hat man das schon experimentell bewiesen? Hat es jemals solch eine stark reduzierende methan-ammoniak-wasserstoff-reiche Uratmosphäre gegeben, in der die nötigen Aminosäuren durch Zufall, Blitzschläge und UV-Strahlung entstehen konnten?
D. E. Hull von der California Research Corporation in Richmond, California (USA), über die Aminosäuren, die in der reduzierenden Uratmosphäre entstanden sein können, und wieviel davon das Urmeer erreicht hätten: "... 97 Prozent des Glyzins (= eine Aminosäure) wäre zerfallen, bevor es die Oberfläche (des Meeres oder der Erde) erreicht hätte." (1960) S. 693
Wie lange etwa hätten sich die 3% der Aminosäuren, die die Oberfläche des Urmeeres erreicht hätten, dann erhalten können? Hätte dort aus diesen Aminosäuren dann eine dicke Suppe entstehen können, so reichhaltig wie eine kräftige Fleischbrühe? Dies ist für uns wichtig, weil sich aus dieser toten chemischen Ursuppe die erste Zelle entwickelt haben soll, und aus dieser ersten Zelle dann alles spätere Leben.
D. E. Hull: " In der gemischten Schicht über der Pyknolinie, etwa 100 Meter
tief, hätte das Glycin dann eine Halbwertzeit gegenüber der ultravioletten Zerstörung von etwa zwanzig Jahren gehabt." (1960) S. 693
Aber das Urmeer muss doch an vielen Stellen bestimmt viel tiefer gewesen sein, als nur 100 Meter! Die Aminosäuren, wie das Glycin, hätten sich bestimmt in Hunderttausenden von Jahren zu einer kräftigen Suppe anreichern können, wo das Urmeer tiefer als 100 Meter war!
D. E. Hull: "Selbst wenn man annähme, dass sie (die Aminosäuren) bis zum Grunde des Meeres hin verteilt wären, mit einer durchschnittlichen Tiefe von 4 km, dann wäre die Halbwertzeit nur 1000 Jahre gewesen. Da (die Aminosäuren) nur so kurz bestehen und dann wieder in der Atmosphäre oder im Ozean zerfallen, konnten sich keine brauchbaren Mengen an organischen Verbindungen in einer Ewigkeit von Zeiten ansammeln." (1960) S. 694
Philipp H. Abelson von der Carnegie Institution von Washington, Washington, D.C., vom Geophysikalischen Laboratorium, hat auch die "chemische Evolution" und ihre angenommene methan-ammoniak-reiche Uratmosphäre, die sie für das Leben brauchte, näher untersucht. Er schreibt:
"Die Hypothese von der frühen Methan-Ammoniak-Atmosphäre ist ohne jede Grundlage und ist stattdessen widerlegt. Wenn die Methan-Ammoniak-Hypothese stimmte, sollte es geologische Beweise dafür geben. Welchen Beweis für eine Ur-Methan-Ammoniak-Atmosphäre auf der Erde hat man? Die Antwort lautet: Man hat keine Beweise dafür; aber es gibt viel, was dagegen spricht. Die Methan-Ammoniak-Hypothese ist in großer Schwierigkeit, soweit es die Sache mit dem Ammoniak betrifft, denn Ammoniak auf der Ur-Erde wäre schnell verschwunden."
Wie schnell wäre das Ammoniak etwa in der Uratmosphäre zerstört worden?
Philipp H. Abelson: "Wenn soviel Ammoniak (in der Uratmosphäre) enthalten wäre, wie heute Stickstoff in der heutigen Atmosphäre, dann würde es (das Ammoniak) in 30 000 Jahren zerstört werden. Kleine Mengen an Ammoniak hätten sich wieder gebildet; aber dieser Vorgang ist unwichtig im Vergleich zu den Mengen, die vernichtet werden." (1966) S. 1365
Die Uratmosphäre soll auch viel Methan enthalten haben. Hat es wenigstens davon viel gegeben?
Philipp H. Abelson: "Wenn es jemals große Mengen an Methan in der Erdatmosphäre gegeben hat, sollte es dafür geologische Beweise geben. Laboratoriumsversuche zeigen uns, wenn eine dichte, stark reduzierende Atmosphäre bestrahlt wird, entstehen hydrophobe organische Moleküle, die von sinkendem Lehm aufgesogen werden. Die ältesten Gesteine sollten daher eine ungewöhnlich große Menge an Kohlenstoff von organischen Chemikalien enthalten. Das ist nicht der Fall." (1966) S. 1365
Warum soll die Uratmosphäre eigentlich nicht viel Methan enthalten haben, wie das von der chemischen Evolution her nötig ist?
P. H. Abelson: "Die Zusammensetzung der Gase Neon, Argon, Krypton und Xenon in der heutigen Atmosphäre ist entscheidend. Neon ist auf der Erde in einer Menge von etwa 10-10 vorhanden, soviel wie im Weltraum, und auch Argon, Krypton und Xenon sind recht selten. Es ist wahrscheinlich, dass, wenn sich Xenon mit einem Atomgewicht von 130 nicht ansammeln konnte, andere flüchtige leichte Stoffe, wie Wasserstoff, Stickstoff, Methan und Kohlenmonoxyd damals auch verschwunden wären. Die Ansicht, dass die Erde eine dichte Methan-Ammoniak-Atmosphäre hatte, wird nicht durch die Geochemie bestätigt, und sie wird durch die Seltenheit von Xenon und Krypton in unserer heutigen Atmosphäre widerlegt." (1966) S. 1365
A. G. Cairns-Smith ist Haupt-Unterweiser für Chemie an der Universität von Glasgow in Schottland. Auch er hat die Hypothese der "chemischen Evolution" viele Jahrzehnte lang erforscht. Er hat auch den sowjetischen Biochemiker und Evolutionisten A. I. Oparin gekannt. -Was hat Professor A. G. Cairns-Smith inzwischen über die angeblich stark reduzierende Uratmosphäre herausgefunden, in der die Lebensbausteine von selbst entstanden sein sollen?
Er schreibt: "Nach Walker (1976) ist die Uratmosphäre die meiste Zeit über nur schwach reduzierend gewesen, als sich alles soweit beruhigt hatte, dass Leben bestehen konnte; er sagt: 'Eine reduzierende Atmosphäre, falls es sie jemals gegeben haben sollte, war nur von kurzer Dauer und endete gewaltsam', und er nimmt an, dass die Uratmosphäre wie unsere Atmosphäre jetzt gewesen ist, nur ganz ohne Sauerstoff, mit ein paar Prozent mehr Wasserstoff." Cairns-Smith, A. G. (1981) S. 16
Hat es im frühen Präkambrium jemals eine Uratmosphäre gegeben, die viel Methan enthielt, so dass sie die Meere mit den nötigen organischen Molekülen versorgen konnte, wie sich das Oparin, Eigen, von Ditfurth, Sagan und andere so vorgestellt haben?
Prof. A. G. Cairns-Smith: "In solch einem ungewissen Gebiet wie diesem sollten wir nicht dogmatisch sein: aber in Obereinstimmung mit der Skepsis von Abelson (1966) und Sillen (1965), findet die Ansicht, dass das Leben in einer methan-reichen Atmosphäre entstanden sei, wo die Meere reich an organischen Molekülen waren, wenig Unterstützung durch die Astronomie und Geologie. Die Atmosphäre könnte wohl neutral gewesen sein -hauptsächlich N2 und CO2. In diesem Falle könnten trotzdem stellenweise organische Moleküle aus CO2 entstanden sein, durch die Einwirkung starker Energie des ultravioletten Lichtes, das die sauerstofflose Atmosphäre durchdringt. Aber dieselbe Strahlung würde verhindern, dass sich große 'Nahrungsvorräte' ansammelten: sie zerbricht und macht organische Moleküle (Rein, et al. 1971)." (1981) S. 16
"Es gibt direkte Beweise dafür, dass es niemals eine stark reduzierende Atmosphäre gegeben hat, bis vor 3,8 Milliarden Jahren. In Grönland gibt es veränderte Sedimentgesteine dieses Alters (Moorbath, O 'Nion & Panhorst, 1973). Diese enthalten reichlich Kohlenstoffe (Allaart, 1976), was beweist, dass es mindestens damals schon Kohlendioxyd in der Atmosphäre gegeben haben muss (Schidlowski, 1978). Da die Grönland-Gesteine nicht allzu unnormal sind, nimmt Moorbath (1977) sogar an, dass die Bedingungen, unter denen sie abgesetzt wurden, nicht viel anders gewesen sein konnten als heute." Cairns-Smith, A. G. (1982) S. 16, 17
Bei den Versuchen von Stanley Miller und seinen Nachfolgern ging man davon aus, dass die Uratmosphäre, in der die Bausteine des Lebens entstanden sein sollen, viel Methan, Ammoniak und Wasserstoff enthielt. -Wie ist das mit dem vielen freien Wasserstoff. -Hat die Atmosphäre im Frühpräkambrium viel freien Wasserstoff enthalten?
Francis Crick erhielt 1962 zusammen mit James Watson und Maurice Wilkins den Medizin-Nobelpreis für die Entdeckung der Molekular-Struktur der Desoxyribonukleinsäure (DNS). Seit 1977 ist er Professor am Salk-lnstitut für Biologische Forschung in San Diego, Kalifornien und an der Universität von San Diego. Er schreibt über den großen Anteil des freien Wasserstoffs in der Uratmosphäre:
"In neuerer Zeit sind diese Vorstellungen angezweifelt worden. Wasserstoff ist so leicht, dass die Schwerkraft der Erde nicht stark genug ist, ihn festzuhalten, und er ohne weiteres in den Weltraum entweicht. In welchem Umfang das geschieht, hängt von einigen Faktoren ab, insbesondere von der Temperatur in der oberen Atmosphäre, denn je höher die Temperatur ist, um so schneller bewegen sich die Atome und Moleküle, und um so leichter entweichen sie in den Weltraum. Heute hält man es für möglich, dass ein Großteil des ursprünglichen Wasserstoffs so schnell entwich, dass er nie die Atmosphäre beherrschte." Crick, F. (1983) S. 83
Hat es jemals eine methan-ammoniak-wasserstoff-reiche Uratmosphäre im frühen Präkambrium gegeben, in der die erste Zelle von selbst entstehen konnte? Hätte diese Uratmosphäre die Bausteine für die erste Zelle liefern können? Wie war sie chemisch zusammengesetzt?
Professor Klaus Dose und Horst Rauchfuß: "Verschiedene Autoren vertraten die Auffassung, dass die primordiale oder primitive Atmosphäre der Erde (d. h. der Atmosphäre der präbiotischen Erde) hauptsächlich Wasserstoff, Methan, Ammoniak und Edelgase enthielt (Russel, 1935; Oparin, 1938; Urey, 1952; Miller and Urey, 1959). In der Tat bestehen 80% der kosmischen Materie aus Wasserstoff; Helium und Wasserstoff zusammen bilden mehr als 90% der Materie des Universums." (1975) S. 50
Hat die Uratmosphäre hauptsächlich aus Methan, Ammoniak und freiem Wasserstoff bestanden?
Professor K. Dose und H. Rauchfuß: "Wäre Wasserstoff und Helium nicht zusammen mit anderen flüchtigen Stoffen während der Bildung der Erde in den Weltraum entwichen und hätte die Temperatur der primordialen Atmosphäre niemals 25°C erheblich überschritten, dann wäre eine Methan-Ammoniak-Wasserdampf-Atmosphäre ... wahrscheinlich.
Diese Vorstellungen sind jedoch geologisch unrealistisch, weil der Überwiegende Teil der primordialen Gase (primäre Atmosphäre) während der Bildung der Erde wieder zurück ins Universum diffundierte. Während der Bildung der jungen Erde erreichte die Erdkruste wahrscheinlich nur noch Temperaturen von 200 bis 1000oC, so dass hier kein allgemeines Schmelzen der Gesteine einsetzte (Urey, 1962). Damit sich aber signifikante Mengen an biochemischen Molekülen auf der Erdkruste anhäufen konnten, musste die durchschnittliche Oberflächentemperatur zunächst auf etwa das gegenwärtige Niveau fallen. Die meisten biochemischen Verbindungen sind bei höheren Temperaturen nicht über geologische Zeiträume stabil." Dose und Rauchfuß (1975) S. 50, 52
"In der ersten Phase der Bildung der jungen Erde dürften vor allem freier Wasserstoff und Helium in den Weltraum diffundiert sein. In der folgenden Phase des Aufbaus einer 'sekundären' Atmosphäre durch vulkanische Ausgasungen können zwar Methan und Ammoniak neben Wasserdampf höhere Konzentrationen in der Atmosphäre erreicht haben, aber vor allem Methan und Ammoniak dürften in der folgenden Zeit durch strahlen und photochemische Reaktionen unter Beteiligung von Spaltprodukten des Wassers (insbesondere von OH-Radikalen) langsam zu CO2, CO und N2 oxidiert worden sein. Abelson (1966) kommt zu dem Schluss, dass die primordiale Atmosphäre der Erde kein Ammoniak enthielt, weil dessen Halbwertzeit aufgrund der ultravioletten Strahlung der Sonne nur etwa 30000 Jahre beträgt. Nach Abelson kann die Atmosphäre der primordialen Erde in der Obergangsphase Protoerde - Erde auch keine größeren Mengen an Methan enthalten haben, weil diese Gase unter der Einwirkung von Strahlung teilweise auch in höhere Kohlenwasserstoffe umgewandet worden wären. Diese Kohlenwasserstoffe hätten bei unmittelbarem Einfluss im Urgestein bis heute überdauern können. Wie Abelson hervorhebt, enthalten die älteren Steine jedoch keine signifikanten Mengen an organischen Verbindungen.
"Man muss daraus schließen, dass die primäre Atmosphäre, die wahrscheinlich überwiegend aus Wasserstoff, Methan, Ammoniak und Wasserdampf bestand, bereits vor dem Abschluss des Bildungsprozesses der jungen Erde verloren gegangen war. Eine signifikante Anhäufung von organischen Verbindungen konnte daher nur durch die Einwirkung verschiedener Energieformen auf die sekundäre Atmosphäre der Erde bewirkt werden." Dose und Rauchfuß (1975) S. 52
Demnach hatte die chemische Evolution also keine methan-ammoniak-wasserstoff-reiche Uratmosphäre, in der die Amino- und Nukleinsäuren -die Bausteine der ersten Zelle -von selbst entstehen konnten. Dann konnten sich auch nicht genug Amino- und Nukleinsäuren im Urmeer oder -teich angesammelt haben, weil die methan-ammoniak-reiche Atmosphäre schon verschwunden war, bevor die Erde ganz fertig aufgebaut war, und bevor unser Erdball sich so weit abgekühlt hatte, dass die organischen Moleküle eine Zeit lang im Ozean oder Teich überleben konnten. -Woraus hat dann die sekundäre Atmosphäre der Erde bestanden? Wie lange hat sie sich etwa halten können?
Professor Dose und Rauchfuß: "Revelle (1965) und andere vermuten, dass die primitive (sekundäre) Atmosphäre Kohlenstoff vor allem in Form von Kohlenmonoxid und Kohlendioxid enthielt. Kohlenmonoxid ist jedoch aus thermodynamischen Gründen in Gegenwart von Wasser nicht stabil. ... Die Halbwertzeit des Kohlenmonoxids bei Raumtemperatur und pH-Wert von 8 beträgt dann wegen der hohen Aktivierungsenergie für diese Reaktion in Abwesenheit eines Katalysators etwa 70000 Jahre; diese Halbwertzeit ist in geologischen Maßstäben gemessen nicht groß. In Gegenwart mineralischer Katalysatoren dürfte sie noch erheblich niedriger liegen." Dose und Rauchfuß (1975) S. 52
CHEMISCHE URSUPPE
Die erste Zelle, so meint Professor Manfred Eigen, habe sich von selbst in einer "Ursuppe" entwickelt, die "so gehaltvoll" gewesen sei, "wie eine kräftige Fleischbrühe" (1981) S. 39, 40. -Wie unsere Forschungen ergeben haben, kann es aber im frühen Präkambrium überhaupt keine methan-ammoniak-reiche stark reduzierende Atmosphäre gegeben haben, die die nötigen Lebensbausteine für die erste Zelle hätte liefern können, und die Aminosäuren hätten sich überhaupt nicht im Urmeer zu einer "gehaltvollen" chemischen Suppe ansammeln können, auch nicht in einem 'kleinen flachen Teich an der Küste des Meeres und auch nicht am Rande eines heißen Vulkans. -Die nötigen Zutaten fehlten.
Nehmen wir jetzt aber an -entgegen all den Tatsachen, die wir bis jetzt kennen -, es hätte wirklich. Solch eine chemische Ursuppe gegeben, oder solch kleinen flachen Teich am Rande des Meeres oder am Rande eines heißen Vulkans: Was dann? Hätte sich wenigstens dann von selbst eine lebende Zelle durch Naturgesetze oder durch einen dialektischen Kampf aus lebloser Materie entwickeln können? Wenn ja: welche experimentellen und fossilen Beweise gibt es dann dafür? Hätte sich solch eine "chemische Suppe" in Hunderten von Millionen von Jahren ansammeln können?
P. H. Abelson: "Arginin zum Beispiel wird von sinkendem Lehm aufgesaugt, ebenso wie Chlorophyll und Porphyrine. Fettsäuren aus unlöslichen Salzen ( würden sich) mit Magnesium und Kalium (verbinden), und wären dadurch der Suppe entzogen. Mindestens fünf wichtige Faktoren begrenzen die Arten der Verbindungen, die sich im Urozean angesammelt haben könnten. Erstens, was man auf anorganische Weise machen kann, hat seine Grenzen; zweitens, alle organischen Stoffe zerfallen mit der Zeit von selbst; drittens, einige Stoffe werden leicht durch die Strahlung zerstört; viertens, viele Verbindungen würden dem Ozean durch Niedersinken und Ansaugen entzogen werden; fünftens, es gibt da schwerwiegende chemische Unverträglichkeiten zwischen den Bestandteilen der lebenden Materie, und einige Bestandteile der Suppe würden reagieren und nicht-biologische Stoffe bilden." (1966) S. 1369
Lars Gunnar Sillen vom Königlichen Institut für Technologie, Abt. für Inorganische Chemie, in Stockholm, Schweden, über die chemische Ursuppe:
"... vernünftige Mengen an organischen Stoffen würden thermodynamisch unstabile Bedingungen voraussetzen... Man kann sich leichter vorstellen, wie sie zerstört werden, als wie sie sich -ohne Leben-, hätten bilden können." (1965) S. 455
Klaus Dose von der Johannes-Gutenberg-Universität in Mainz, am Institut für Biochemie, ist einer der führenden Fachmänner für chemische Evolution. -Hätte es überhaupt solch eine "gehaltvolle" chemische Ursuppe geben können, wie eine "kräftige Fleischbrühe", in der sich die erste Zelle auf der Erde von selbst entwickeln konnte? Hätten sich die Aminosäuren und die anderen nötigen Moleküle in Hunderten von Millionen von Jahren in den Urmeeren so weit anreichern können, dass eine "chemische Suppe" daraus entstanden wäre?
Klaus Dose: "Solch eine Konzentration ist viel zu gering für die direkte Bildung von Polymeren und komplizierteren Strukturen. Man könnte sie mit der Konzentration von freien Aminosäuren im heutigen nordatlantischen Ozean vergleichen... Es ist deshalb wahrscheinlich, dass die mittlere Konzentration an freien Aminosäuren im Urozean nicht viel höher gewesen ist als heute." (1974) S. 74
Hätten diese Amino- und Nukleinsäure-Ketten von selbst in der chemischen Suppe entstehen können?
Klaus Dose: "Die Wahrscheinlichkeit, dass Polypeptide und Polynukleotide in einem wässrigen System überleben können, ist viel geringer als bei den freien Aminosäuren. ... Man weiß nicht, wie Polypeptide entstehen könnten, so dass genug Peptide im Ozean vorhanden wären, etwa 1% der Lösung, damit präbiotische Systeme von selbst entstehen könnten." (1974) S. 74.
"Wir kommen daher zu dem Schluss, dass der Urozean große Mengen an Aminosäuren und anderen Arten von Molekülen enthalten haben könnte, die für das Leben wichtig sind; aber ihre Konzentration war zu gering, als dass dort präbiotische Systeme hätten entstehen können." Dose, K. (1974) S. 74.
"Dass sich verschiedene Arten von biochemischen Verbindungen in großen Teilen der Urgewässer hätten ansammeln können, ist jedoch sehr unwahrscheinlich, aus mehreren Gründen. Erstens, Aminosäuren, Aldehyde, Cyanide, und andere solche reagierenden Stoffe sind in wässrigen Lösungen besonders unstabil. Zweitens, die meisten Stoffe, die da entstehen, sind von den biologisch wichtigen Molekülen recht verschieden. Drittens, der Urozean wurde ständig von einer recht hohen Menge ultravioletten Sonnenlichtes bestrahlt. Eine ständige Bestrahlung einer recht gleichförmigen Lösung führt zu abbauenden, statt zu aufbauenden Reaktionen: schließlich wird ein photochemisches Gleichgewicht erreicht. ... Die Vorstellung von einer primitiven 'dicken Suppe' oder 'Ur-Fleischbrühe' ist eine der hartnäckigsten Ansichten, die sehr klar widerlegt wird durch thermodynamische Oberlegungen und durch einen Mangel an experimentellen Beweisen." Fox, S. W. & K. Dose (1977) S. 37, 38
"Bei der Synthese eines Peptids muss man auf jeden Fall das Wasser entfernen und freie Energie hinzufügen..." Dose, K. (1983) S. 919
J. Brooks und G. Shaw über die "chemische Suppe", die für Oparins und Eigens Evolutionstheorien nötig ist, und die sedimentären Beweise, die man bis jetzt dafür gefunden hat:
"... es gibt keine Beweise dafür, dass es jemals eine 'Ursuppe' für irgendeine längere Zeit gegeben hat. Wenn es diese 'Suppe' jemals gegeben hätte, wäre es gemäß der chemischen Evolution unbedingt nötig gewesen, dass sie große Mengen an stickhoffhaltigen organischen Verbindungen (Aminosäuren, Nukleinsäurebasen, usw.) enthält. Solche Stoffe werden in Laboratoriums-Versuchen leicht von sinkenden anorganischen Teilchen angesogen, und würden daher unter gewöhnlichen geologischen Bedingungen und in einer Umwelt, die kein Leben enthielt, zweifellos zusammen mit den Gesteins und Mineral-Teilchen zu Boden sinken." (1978) S. 604
"Dadurch hätten dann große Gebiete mit Ablagerungen entstehen müssen, die organische Verbindungen enthalten -da die Theorie von der chemischen Evolution voraussetzt, dass große Mengen von solchen Verbindungen über lange Zeit hinweg vorhanden waren, so dass der Zufall Gelegenheit hatte, die verschiedenen chemischen Vorgänge zu beeinflussen, die dann angeblich zu lebenden Systemen geführt haben sollen." Brooks, J. & G. Shaw (1978) S. 604
Es wäre natürlich unvermeidlich, dass solche Sedimente sich ganz normal
veränderten, und wir sollten dann erwarten, dass wir bedeutende Mengen an Koksen ('nitrogenen Koksen'), die aus Stickstoff entstanden sind, vorfinden, die in den verschiedenen Sedimenten eingefangen wurden. Solche 'Kokse' entstehen heute ganz normal, wenn man organische Stoffe, die viel Stickstoff enthalten, erhitzt. Solche Stoffe sind bis jetzt aber noch nicht in präkambrischen Gesteinen auf diesem Planeten gefunden worden. Das Gegenteil scheint der Fall zu sein." Brooks, J. & G. Shaw (1978) S. 605.
Wie viel Stickstoff enthält die organische Masse in präkambrischen Schicht-gesteinen gewöhnlich?
J. Brooks & G. Shaw: "Der Stickstoffgehalt in der präkambrischen organischen Masse ist sehr gering (0,2%). Die unlösliche organische Masse ( 'Kerogen' ), die in den präkambrischen Sedimenten gewöhnlich enthalten ist, enthält gewöhnlich vorwiegend Kohlenstoff, Wasserstoff und Sauerstoff, mit sehr wenig organischem Stickstoff oder Schwefel." (1978) S. 604
Was schießen Sie daraus?
J. Brooks & G. Shaw: "Es hat niemals irgendwelche bedeutende Mengen von einer 'Ursuppe' auf der Erde gegeben, als sich die präkambrischen Sedimente bildeten... Wenn es wirklich solch eine ’Suppe’, gegeben haben sollte, dann nur für ganz kurze Zeit. ... Die geochemischen Untersuchungen deuten darauf hin, dass es im ganzen frühen Präkambrium reichlich Beweise dafür gibt, dass lebende Systeme schon lebten, als sie abgelagert wurden, und dass sie photosynthetisierenden biochemischen Reaktionen unterworfen waren, wie die heute lebenden Systeme auch." (1978) S. 605
Professor H. Follmann schreibt über die "chemische Suppen, ihren Inhalt und ihre Konzentration:
"Eine der großen Unbekannten im präbiotischen Geschehen sind die Konzentrationen der organischen Verbindungen in den Urozeanen. Sie bestimmen über Geschwindigkeit und Richtung der Reaktionen, aber können in unseren Laborexperimenten, bei denen in begrenzter Zeit immer nur wenige Prozent Stoffumsatz und wenige Substanzen nebeneinander vorkommen, nicht gut simuliert werden. Sehr gehaltvoll kann die Ursuppe jedenfalls nicht gewesen sein: Selbst wenn alle heutige organische Materie im Volumen der Ozeane gelöst wäre, entstände nur eine l %ge Lösung!
"Frühere Vorstellungen, nach denen sich bei laufender Neubildung über Jahrmillionen hinweg eben doch hohe Konzentrationen an Biomolekül Vorstufen anreichern sollten, haben übersehen, dass aus Lösungen von Aldehyden, Aminosäuren und Zuckern rasch und irreversibel humusartige, kondensierte, schließlich zu Boden sinkende Produkte entstehen, die weder chemisch noch biologisch weiterzuverwerten sind. Fettsäuren fallen als Caliumsalze, Porphyrine absorbieren sich an Sedimente. ... Dass sich die Organisation von Monomeren zu Makromolekülen und höheren Strukturen bei derartigen Konzentrationen vollziehen konnte, ist sehr unwahrscheinlich." Follmann, H. (1981) S. 66, 67
"Ein Gemisch organischer Substrate macht noch keinen Stoffwechsel, und ein paar Nucleotide zusammen keine Erbinformation." Follmann, H. (1981) S. 67
A. G. Cairns-Smith über die "Ursuppe" in flachen Teichen und über die
Zeit, in der sich die erste Zelle hätte entwickeln können: "Man kann vernünftigerweise annehmen, dass eine ozeanische Suppe nicht nötig war, sondern dass man statt dessen einen Vorrat an organischen Molekülen brauchte, die von der richtigen Art waren; dadurch sollten sie dann irgendwie die nötige Konzentration erreicht haben, und logischerweise sollten sie mit den Stoffen geliefert werden, die für die ersten sich entwickelnden Systeme nötig waren, und sie mit Nahrung versorgen. Vielleicht hat es am Rande des Ozeans einen verdunstenden Tümpel gegeben, in dem sich die Stoffe konzentrieren konnten. Man muss aber erst viel verdampfen, bevor man von (einem Gehalt) von 10-7 M auf die Art von Konzentration kommt, die man vielleicht gebraucht hat. Und das ultraviolette Licht hätte auch gestört, während sich (die Suppe) konzentrierte, indem sie verdunstete." (1982) S. 48
Wie lange hätten sich die Chemikalien in der Ursuppe im frühen Präkambrium konzentrieren können?
A. G. Cairns-Smith: "Es gibt Beweise dafür von Mondgesteinen und von anderswo, dass damals viele Krater durch Einschläge entstanden, und zwar überall im inneren Sonnensystem, die vor etwa 4,0 Milliarden Jahren aufhörten. Damals war anscheinend die letzte Phase, in der die inneren Planeten wuchsen; dadurch erhalten wir das frühest mögliche Datum, an dem das Leben entstanden ist (oder für den Aufbau der Ursuppe, falls es so etwas jemals gegeben hat). Wenn eine stark reduzierende Atmosphäre für den Ursprung des Lebens nötig war, dann waren nur etwa 0,2 Milliarden Jahre vorhanden, in denen es sie gegeben haben konnte." (1982) S. 17
"Organische Stoffe können eher organisiert werden. Wenn zwei Kohlenstoffatome erst einmal richtig zusammengesetzt worden sind, mögen sie für immer zusammenbleiben. Gerade deshalb gibt es für die automatische Fehlerverbesserung viel weniger Spielraum: die Fehler bleiben auch. Gewöhnlich braucht man einen tüchtigen organischen Chemiker oder ein Enzym, um teeriges Chaos zu vermeiden. Deshalb stimmt es nur zum Teil, wenn man oft sagt, dass organische Moleküle ideal seien, um damit die biomolekulare Maschinerie zu bauen. Organisierte Moleküle sind für das Leben ideal, in der Art und Weise, wie eine Geige dafür ideal ist, damit Musik zu machen -in den Händen eines Experten, der die Vielfalt der Möglichkeiten richtig nutzen kann. Organische Moleküle sind ideal für entwickeltes Leben, aber das erste Leben konnte noch nichts davon wissen. Ich glaube, dass, wie so viele Anfänge, auch die Anfänge der organischen Evolution etwas Besonderes gewesen sind." Cairns-Smith, A. G. (1982) S. 31
Warum sollen die Anfänge des Lebens etwas Besonderes gewesen sein?
A. G. Cairns-Smith: "Die ersten Monomere wären stark verunreinigt gewesen. Aus Simulierungs-Experimenten weiß man, dass sie dort in einer komplexen Mischung vorhanden gewesen wären, die viele verschiedene reagierende Moleküle enthielt. Kein vernünftiger organischer Chemiker wird erwarten, dass er viel an Rekationen von Ausgangsstoffen bekommt, die aus Teeren bestehen und die nur wenige richtige Reagenten enthalten. Vielleicht, weil sie vernünftige organische Chemiker sind, beginnen die meisten Experimentatoren nicht mit solch komplexen Mischungen, wenn sie herausfinden wollen, wie Biopolymere von selbst entstanden sind." (1982) S. 45, 46
Gibt es noch andere Probleme in der "chemischen Evolution"?
Cairns-Smith: "Die Bedeutung der ultravioletten Strahlung, die die organischen Moleküle zerstört, wurde erneut von Rein, Nir & Stamadiadou (1971) hervorgehoben. ... Dose zeigt uns, dass die Konzentration der Aminosäuren in der 'Suppe' etwa so hoch gewesen sei, wie in den Ozeanen heute. Zu einem ähnlichen Schluss kommt Nissenbaum (1976) aufgrund anderer (nicht-biologischer Vorgänge), die organische Moleküle im Ozean vertilgen, indem sie sich mit sinkenden Stoffen verbinden.
"Deshalb bestehen die organischen Moleküle 1000-3000 Jahre. Eine weitere Auswirkung, die man jetzt auf dem Mars beobachten kann, würde die Oberfläche (der Erde) frei von organischen Molekülen gehalten haben. Ultraviolette Strahlung, die eine sauerstofffreie (oder -arme) Atmosphäre durchdringen kann, kann sich oxidierend auf anorganisches Oberflächen-Material auswirken, wobei sie Sorten erzeugt, die bereit sind, jedes organische Molekül zu vernichten, das sich gebildet hat (Ponnamperuma et al., 1977; Klein, 1978)." Cairns-Smith, A. G. (1982) S. 46, 47
"... alle wichtigen Biopolymere in wässriger Lösung können sich im Verhältnis zu ihren (deaktivierten) Monomeren verändern. Das Polypeptid wird sich im Wasser in seine Bestandteile, in Aminosäuren, auflösen: Miller & Orgel (1974) schätzen, dass die Halbwertzeit von Alanylanin etwa 8 x 107 Jahre bei 0°C beträgt, und etwa 6 x 105 Jahre bei 25°C." Cairns-Smith, A. G. (1982) S. 48
"Es scheint mir, dass die Ansicht, Haftvermittler (coupling agents) würden in einer leblosen Welt Polypeptide zusammenstellen, eine weitere Unwirklichkeit einem schon unwirklichen Gedanken hinzufügt. Erinnern Sie sich bitte daran, dass Versuche, die die Urzeit nachahmen sollen, gewöhnlich nur wenige Aminosäuren erzeugen. Erinnern Sie sich bitte daran, dass die Produkte, (die dabei entstehen), Teere sind, und dass Vorschläge darüber, wie das Leben entstanden sein soll, gewöhnlich fehlen. Erinnern Sie sich bitte daran, wie schwierig es ist, Lösungen von Aminosäuren oder von Cyaniden oder Phosphaten in Konzentrationen herzustellen, wenn man Haftvermittler (coupling agents) macht. Erinnern Sie sich bitte daran, dass diese Mittel selbst dann nicht sehr gut arbeiten, wenn man sie aus Labor-Flaschen nimmt." Cairns-Smith, A. G.
(1982) S. 52, 53
"Es ist ebenfalls schwierig, sich vorzustellen, dass Polysaccharide sich im Urwasser anhäufen könnten. Die Monosaccharide konnten, wie wir gesehen haben, nur leicht aus Formaldehyd hergestellt werden, soweit man bis heute weiß, und es ist zweifelhaft, ob sie in genügender Konzentration vorhanden gewesen sein konnten. Das Produkt der Formose-Reaktion ist in jedem Fall, wie wir uns erinnern werden, eine sehr komplexe Mischung, aus der dann leicht höhere Polymere und Karamel entstehen kann." Cairns-Smith, A. G. (1982) S. 55
Was haben andere Forscher inzwischen über den Ursprung der ersten Zelle herausgefunden? Wie wahrscheinlich ist es, dass sie sich von selbst in einer chemischen Ursuppe entwickeln konnte?
P. Karlson schreibt in seinem Lehrbuch für Biochemie:
"Proteine können sich nicht aus den freien Aminosäuren durch Umkehrung der Proteolyse bilden. Wir haben betont, dass das Gleichgewicht ganz weit auf seiten der Hydrolyse (= Kettenspalten durch Wasser) liegt, Peptide also leicht in Aminosäuren aufspalten. Aminosäuren aber nicht zu Peptiden zusammentreten. Hierzu muss die Aminosäure zunächst 'aktiviert " d.h. auf ein höheres Gruppenübertragungspotential gehoben werden. Die dafür notwendige chemische Energie wird von Adenosintriphosphat (ATP) geliefert. Für jede Aminosäure existiert mindestens ein spezifisches aktivierendes Enzym und mindestens eine spezifische Transfer-RNS. Die Substanzen, die diese recht komplexe Reaktion ermöglichen, sind also Enzyme und Transfer-RNS, die sich aus Blitzen, Ammoniak, Wasserdampf und Methan nicht bilden lassen. Die Synthese von Peptiden und Proteinen in einer Ursuppe wäre auch aus diesem Grunde chemisch gesehen unmöglich." Wilder Smith, A. E. (1980) S. 146
Sir Fred Hoyle zu der Frage: Konnte die erste Zelle von selbst in der "chemischen Ursuppe" entstehen? -Er schreibt:
"... es gibt nicht den geringsten stichhaltigen Beweis für die Hypothese,
dass das Leben in einer organischen Suppe hier auf der Erde entstanden ist. Francis Crick, der sich einen Nobelpreis (mit einem anderen Forscher) teilt, weil er den Aufbau der DN A entdeckte, ist ein Biophysiker, den diese Theorie nicht überzeugt. Weshalb schwelgen Biologen dann in unbegründeten Fantasien, um zu leugnen, was doch so offensichtlich ist, dass die 200 000 Aminosäure-Ketten, und damit das Leben, nicht durch Zufall entstanden sind?" (1983) S. 22, 23
ERGEBNIS
1. Es gibt überhaupt keine fossilen und experimentellen Beweise dafür, dass es jemals eine "kräftige chemische Suppe" hier auf der Erde gegeben hat, in der die erste Zelle von selbst entstehen konnte. Die Hypothese von der "chemischen Evolution", nach der sich die erste Zelle nur durch Naturgesetze aus lebloser Materie von selbst entwickelt haben soll, widerspricht allem, was man bis jetzt über Chemie und Physik weiß. Sie ist nur freie wissenschaftliche Dichtung (Science Fiction), die man im Namen der Wissenschaft verbreitet hat, um ihr Ansehen zu erhöhen.
2. Die "chemische Suppe" hätte sich überhaupt nicht im frühen Präkambrium bilden können, weil es keine geeignete Atmosphäre gab, in der die nötigen Verbindungen entstehen konnten. Selbst wenn es eine stark reduzierende Uratmosphäre gegeben hätte, die viel Methan und Ammoniak enthielt, wäre
damit für die "chemische Evolution" nichts gewonnen: Nur etwa 3% der Aminosäuren, die sich in der Atmosphäre bildeten, hätten die Oberfläche des Urmeeres erreicht. Die übrigen 97% der entstandenen Aminosäuren wären vorher durch die ultraviolette Strahlung zerstört worden.
3. Die Aminosäuren und anderen Verbindungen, die die Oberfläche des Urmeeres erreichten, hätten sich dort nicht zu einer "chemischen Suppe" anreichern können, die so gehaltvoll war wie eine "kräftige Fleischbrühe", wie Manfred Eigen meint, weil sie das Wasser wieder zerlegt hätte. Die Aminosäuren und andere Lebensbausteine wären dann auf den Grund des Meeres oder des kleinen flachen Tümpels am Rande des Meeres gesunken. Sie würden sich dann bald in eine teerige Masse verwandeln, die für das Leben völlig unbrauchbar ist.
4. Es gibt reichlich gut erhaltene frühpräkambrische Fossilien und Sedimente, wie zum Beispiel in den Isua-Gesteinen Westgrönlands und in vielen anderen Teilen der Welt. Sie beweisen uns deutlich, dass es dort keine "chemische Ursuppe" gegeben hat, keine "Vorstufen" des Lebens wie "Koazervat-Tropfen",
"Protobionten" und "Mikrosphären", aus denen sich die erste Zelle entwickelt
haben soll. Es sind von Anfang an nur vollkommene, hochkomplizierte einzellige Organismen gefunden worden, vergleichbar mit unseren heutigen blaugrünen Algen und Hefepilzen.
5. A. I. Oparins und M. Eigens Evolutionstheorien stehen und fallen mit dem Vorhandensein der "chemischen Ursuppe". Dafür haben sie aber überhaupt keine stichhaltigen Beweise. Die nötigen Aminosäuren hätten sich überhaupt nicht in der Atmosphäre bilden können, und sie hätten sich auch nicht im Urmeer zu einer "chemischen Suppe" anreichern können, aus der sich die erste Zelle hätte entwickeln können. Deshalb brechen Oparins und Eigens Evolutionstheorien völlig in sich zusammen. Sie sind jetzt nur noch von geschichtlichem Wert."
Nehmen wir jetzt jedoch einmal an, alle bisher aufgeführten Daten und Argumente seien aus noch unbekannten Gründen null und nichtig, und es hätte auf unserer Erde anfangs doch eine "Ursuppe" 'so gehaltvoll wie eine kräftige Fleischbrühe' gegeben. Auch dann ginge Eigens Ansatz von falschen Voraussetzungen aus.
Ich zitiere dazu im folgenden Bruno Vollmert 1985, pp. 50-58 (Das Molekül und das Leben; Rowohlt Verlag):
"Einfluss des Wassers auf die Kettenlänge
Was im Druckknopfmodell nicht zum Ausdruck kommt, ist die Freisetzung eines Wassermoleküls bei der Bildung einer Estergruppe. Für die Entstehung von Makromolekülen ist das von Bedeutung, denn ebenso wie unter Austritt eines Wassermoleküls die beiden Monomermoleküle durch Bildung der Estergruppe verbunden werden, können sie durch Eintritt eines Wassermoleküls in die Kette unter Rückbildung von OH und Säuregruppen auch wieder getrennt werden (Hydrolyse). Diese Rückläufigkeit der Reaktion wird in Abb. S. 49 durch den Doppelpfeil angedeutet. Sie hat zur Folge, dass in einer Lösung von bifunktionellen Alkohol- und Säuremolekülen nicht alle OH und COOH-Gruppen zu Estergruppen (-COO) + H~O umgesetzt werden, so dass die Ketten nicht beliebig lang werden können. Vielmehr stellt sich ein Gleichgewichtszustand ein, der dann erreicht ist, wenn pro Sekunde ebenso viele Kettenbindungen wieder gespalten werden wie neu entstehen. Quantitativ wird der Einfluss der Wasserkonzentration auf die Kettenlänge durch das auf dem 2. Hauptsatz der Thermodynamik beruhende Massenwirkungsgesetz beschrieben.
Gegen eine Begrenzung der Kettenlänge durch Hydrolyse wurde eingewendet, dass die Erde ein offenes System sei und daher die Gleichgewichtsthermodynamik durch eine Nichtgleichgewichtsthermodynamik * zu ersetzen sei.' Es ist sicher richtig, dass Leben ein Fließgleichgewicht darstellt, was, seit LUDWIG VON BERTALANFFY diesen Begriff einführte, kaum noch jemand bestreiten wird. Das Brunnenbild sagt mehr als viele Worte. Nur: Wie soll das einleuchtende Brunnenmodell auf die Kettenlänge bei einer Polykondensation übertragen werden? Ohne Reparaturenzyme ~~, die auftretende Kettenspaltungen schnell wieder flicken (Risse in dem Brunnengemäuer), dürfte da nichts zu machen sein. Enzyme aber gibt es in der Ursuppe ohne Makromoleküle nicht. Die sollen ja erst entstehen.
Man hat zwar schon an einen ständigen Zufluss von hochreaktiven Monomeren gedacht, wodurch die Kettenwachstumsgeschwindigkeit gegenüber der Abbaugeschwindigkeit stark erhöht wird, jedoch wird dadurch
1. ein durch Hydrolyse angerichteter Schaden nicht behoben (jetzt muss man an die Erhaltung der Sequenz denken), besonders wenn die hydrolytische Spaltung gerade eine selten gute Mutante getroffen hatte;
2. hat in einer wässrigen Lösung (ohne die etwas mysteriösen, aber hochwirksamen Reparaturenzyme) die Hydrolyse immer das letzte Wort, weil sie Ketten statistisch spaltet und an den Spaltstellen nichtaktivierte Endgruppen hinterlässt und insofern die Geschwindigkeit der statistischen Kettenspaltung durch Zufuhr aktiver Monomerer nicht beeinflusst, das heißt nicht vermindert wird, so dass eine (wie auch immer bewirkte) Erhöhung der mittleren Kettenlänge stets eine Erhöhung der Anzahl Spaltstellen pro Kette zur Folge hat, das heißt zu einer rascheren Abnahme der Kettenlänge bei gleichbleibender Anzahl der Spaltereignisse pro Sekunde führt* ;
3. haben hochreaktive Monomere eine mehrstufige Synthesekette zu durchlaufen, so dass ihre Konzentration gegenüber den Primärprodukten aus der Uratmosphäre zwangsläufig sehr gering ist.
Schließlich wird (unabhängig von der Hydrolyse) die Kettenlänge durch das Zahlenverhältnis q der funktionellen Gruppen begrenzt. Davon wird im nächsten Abschnitt die Rede sein.
Was die Nichtgleichgewichtsthermodynamik (Fließgleichgewicht) betrifft, so darf man sich von ihr für das Entstehen und Bestehen langer Ketten in wässriger Lösung (Ursuppe) nicht zuviel versprechen; genaugenommen gar nichts. Jeder, der will, kann sich davon überzeugen, dass lange Kettenmoleküle mit hydrolyseempfindlichen Kettenbindungen (Nucleinsäuren, Proteine) in lebenden Zellen erstaunlich lange stabil sind. Man kann sich aber auch überzeugen, dass sie es nicht mehr sind, wenn man sie aus der lebenden Zelle herausnimmt und sie ihres Enzymschutzes beraubt oder wenn das Lebewesen gestorben ist. Dann wird lebende Substanz wieder zur toten Ursuppe, von selbst (durch Verwesung, Hydrolyse), unter dem Zwang des Massenwirkungsgesetzes. Der umgekehrte Weg, von der Ursuppe zum Leben, wäre der Weg der Selbstorganisation. Die Ursuppe aber ist tot und kennt nur einen Weg, den Weg hin zum thermodynamischen Gleichgewicht.
(Fußnote von B. Vollmert zum thermodynamischen Gleichgewicht:
MANFRED EIGEN: ´Erst wenn der Organismus gestorben ist, streben alle Reaktionen dem Gleichgewichtszustand zu.ª' Das gilt selbstverständlich auch für die noch tote Ursuppe. Damit bestätigt auch EIGEN, dass sich in Ursuppen Makromoleküle wie DNS oder RNS oder Proteine nicht bilden können.)
Man kann die mittlere Gleichgewichtskettenlänge Pu berechnen. Sie liegt bei Wasserkonzentrationen über 80 Prozent in der Größenordnung von Pu = 2, das heißt lange Ketten können sich ohne Fließgleichgewicht nicht bilden. Ein Fließgleichgewicht aber ist nur mit Reparaturenzymen aufrechtzuerhalten, die in der Lage sind, hydrolytische Kettenspaltungen wieder rückgängig zu machen. Reparaturenzyme aber setzen lebende Zellen voraus.""
Auch durch Laboratoriumsversuche mit hochreaktiven Monomeren ist die Gültigkeit des Massenwirkungsgesetzes (Gleichgewichtsthermodynamik) für den Einfluss der Wasserkonzentration auf die Kettenlänge bei Polykondensationsversuchen von Nucleosidphosphaten bewiesen worden."3
Die umfangreichsten experimentellen Erfahrungen mit der Hydrolysestabilität bzw. Hydrolyseanfälligkeit der verschiedensten Nucleosidphosphatmonomeren und Nucleotidoligomeren (das sind kurze DNS-Kettenstücke) sind neueren Datums und stammen aus den gentechnischen Laboratorien. Die Spezialisten, die sich dort mit der Synthese von DNS-Kettenstücken befassen, kennen und behandeln Wasser als ihren Feind, so dass sie es aus Apparaturen und Reagenzien so sorgfältig wie nur möglich entfernen und ausschließen. Gentechnologen bezeichnen Nucleotide und Oligonucleotide als ´chemisch außerordentlich unbeständigª."24.
Quantitativ wird das Gesagte durch folgende theoretisch abzuleitende Gleichung, die den Rang eines Naturgesetzes hat, beschrieben (Ableitung siehe Seite 212ff):
Abb. 20
Sie besagt, dass die Kettenlänge Pn der Wurzel aus dem Produkt von Wasserkonzentration [H2O] und Umsatz p umgekehrt proportional ist. Bei realistisch angesetzten Wasserkonzentrationen von höher als 99 Prozent ergeben sich nach (I) mittlere Kettenlängen von weit unter Pn = 2. Versuche von L. ORGEL haben bestätigt dass bei Wasserkonzentrationen höher als 99,5 Prozent keine Polykondensation von Nucleotiden stattfindet, weil die Kettenspaltung durch Hydrolyse zehn- bis hundertmal schneller verläuft als der Kettenaufbau durch Polykondensation 23 -eine experimentelle Widerlegung von EIGENS Behauptung, die Gleichgewichtsthermodynamik der Gleichung ( I) habe für die Frage der Entstehung des Lebens durch Selbstorganisation keine Bedeutung.
Der Einfluss monofunktioneller Moleküle auf die Kettenlänge
Während der Einfluss des Wassers auf die Kettenlänge durch einfache Modelle nicht zu erklären ist, so dass die Diskussion dieser Frage für den Nichtchemiker verwirrend wirkt, ist der Einfluss monofunktioneller Moleküle auf die Kettenlänge mit Hilfe von Kugelmodellen leicht zu erklären und auf den ersten Blick zu erkennen
Makromoleküle sind lange, kettenförmige Gebilde. Sie entstehen im Grunde nicht anders als gewöhnliche Perlenketten oder Gliederketten, nämlich dadurch, dass ein Kettenglied nach dem anderen an die so immer länger werdende Kette angefügt wird. Nur sind Moleküle unsichtbar klein, so dass sie sich selbst mit der feinsten Pinzette nicht fassen lassen. Das ist aber für das Entstehen der langkettigen Makromoleküle auch gar nicht nötig. Wenn man geeignete Moleküle hat, die man als Monomere bezeichnet, fügen sich diese unter dem Einfluss der Molekularbewegung von selbst zur Kette zusammen. Immer dann tun sie das, wenn die verwendeten monomeren Ausgangsmoleküle bifunktionell sind, das heißt sozusagen zwei klebrige Stellen nach Art eines Klettenverschlusses haben, mit denen sie bei passenden Zusammenstößen aneinander hängen bleiben, so dass zwangsläufig lange Ketten entstehen. Voraussetzung für das Funktionieren dieses Mechanismus ist, dass die Monomermoleküle genau zwei Haftstellen haben. Wenn auch Moleküle dabei sind, die nur eine Haftstelle haben und an der anderen Seite glatt sind, besetzen diese sogenannten Monofunktionellen die Kettenenden, und eine Verlängerung der Ketten ist unmöglich, weil zum wiederholten Einhaken von Molekülen notwendigerweise zwei Haftstellen oder Haftgruppen pro Molekül notwendig sind. Als Modell für die Entstehung einer Makromolekülkette stelle man sich einen Kasten mit Kugeln vor, die an zwei gegenüberliegenden Stellen als Haftstellen zwei Druckknöpfe haben, ein Knopfteil und ein Nutteil.
Solange nur solche Kugeln mit je zwei verschiedenen Druckknopfteilen im Kasten sind, kann man beliebig lange eine Kugel nach der anderen aus dem Kasten holen und sie an die immer länger werdende Kette anfügen. Wenn man aber im Vorratskasten bifunktionelle Kugeln (die je zwei Druckknopfteile besitzen) mit monofunktionellen Kugeln (die nur ein Druckknopfteil haben) mischt und mit dieser Mischung eine Kette zu bauen versucht, scheitert das Unternehmen der Kettenbildung sehr bald. Natürlich darf man nur blind in den Kugelkasten greifen, denn Moleküle haben keine Intelligenz und können nicht auswählen, das heißt alle Zusammenstöße geschehen zufällig. Kugeln mit nicht an die Kettenenden passenden Druckknopfteilen gibt man in den Kasten zurück, denn die entsprechenden Zusammenstöße würden bei Molekülen nicht zu einer Verbindung führen. Herausgegriffene Kugeln, deren Druckknöpfe an eine Seite der im Bau befindlichen Kette passen, werden an die Kette angefügt
Nun kann es sein, dass man Glück hat, indem man zufällig zwei oder dreimal hintereinander eine bifunktionelle Kugel mit zwei Druckknöpfen zu fassen bekommt, ehe man Kugeln mit nur einem Druckknopfteil greift. Dann entsteht eine Kette mit zwei oder drei oder vier Kugeln pro Kette. Die Wahrscheinlichkeit für
das Entstehen von Ketten aus zwei oder drei Kugeln wird aber um so geringer, je größer der Anteil an Kugeln mit nur einem Druckknopfteil in der Ausgangsmischung im Kasten ist. Lange Ketten können sich schon bei geringem Anteil an monofunktionellen Kugeln, das heißt solchen mit nur einem Druckknopfteil, nicht mehr bilden.
Was mit diesem Modellspiel veranschaulicht wird, ist das Gesetz der konstanten Proportionen, auch Stöchiometriegesetz genannt. Dieses Gesetz besagt, dass die Bildung von Makromolekülketten unmöglich ist, wenn sich neben den bifunktionellen größere Anteile an monofunktionellen Molekülen -entsprechend den Kugeln mit nur einem Druckknopfteil -in der Ausgangsmischung befinden, und liefert somit eine klar umrissene naturgesetzliche Bedingung für das Entstehen von Makromolekülen durch Polykondensation.
Will man das Ergebnis solcher Modellexperimente auf eine Formel bringen, so kann man sich wieder der schon mehrfach benutzten Kugelsymbole mit den Druckknopfteilen bedienen, wie in Abb. S. 56. Man wird solche Darstellungen (dasselbe gilt auch von Abb. S. 47 und S. 49) natürlich nicht ´wörtlich" verstehen, das heißt es ist nicht die Anzahl der reagierenden Moleküle (Kugeln) gemeint, sondern das Zahlenverhältnis. Was im Modellbild einmal dargestellt ist, ereignet sich viele Billionen Male in einem Reagenzglas, aber eben immer in dem durch die Reaktionsgleichung oder die Modelle dargestellten Zahlenverhältnis I: I; 5O/ 50, IOOO/ IOOO etc. oder 2: I; 67/33; 2O0/ IOO etc.
Abb. S. 56 zeigt eine bildhaft-symbolische Darstellung dessen,
Abb. 21
Zum Einfluss der Stöchiometrie der Komponenten auf die mittlere Kettenlänge Pn bei Polykondensationen
(I! Bei strengem I: I-Verhältnis der funktionellen Gruppen werden die
Ketten bei vollständigem Umsatz (p = I) unendlich lang
(2! Verschiedene Möglichkeiten des Bi: Mono Verhältnisses:
I Bi: Mono= I: I, ausreichend, um alle x-Gruppen zu blockieren,
Ursuppensituation nach MILLER: Aminosäure: Ameisensäure
(etc.) ~ I:3
2 Bi: Mono = I: I; z. B. Methylamin und Aethylamin blockieren die
Polykondensation von Aminosäuren (Ursuppe!
3 o-Gruppen-Überschuss bei Zweikomponentensystemen (zum Vergleich)
4 Mischung von Monomeren mit beiden Sorten von monofunktionellen Molekülen Bi: Mono = I: 2
5 Mischung mit einer aktivierten (schneller reagierenden) Komponente; Ursuppenbeispiel: Adenosintriphosphat in Mischung mit verschiedenen monofunktionellen Alkoholen, Aminen und Säuren, wobei Säuregruppen (x) langsamer reagieren.
q ist das reale Verhältnis der beiden funktionellen Gruppen bei Zweikomponentenpolykondensationen gemäß Abb. S. 47.
q * ist das äquivalente Verhältnis bei Einkomponentenpolykondensationen(gemäß Abb. S. 49)bei Gegenwart von monofunktionellen Molekülen
was eine theoretisch abgeleitete Gleichung (siehe Seite 57) erwarten lässt, was man sich durch Modellsimulationen mit Druckknopfkugeln handgreiflich klarmachen kann und was durch ungezählte Laboratoriumsexperimente bestätigt worden ist.
In Worten ausgedrückt, sagt die Abbildung: Monofunktionelle Moleküle (Kugeln mit nur einem Druckknopf) brechen die Kette ab. Lange Ketten entstehen nur, wenn monofunktionelle Moleküle ausgeschlossen sind. Ein Überschuss an Monofunktionellen
macht eine Kettenbildung um SO unwahrscheinlicher, je größer der Überschuss ist. *
Das aber bedeutet, dass sich in Ursuppen keine Makromoleküle durch Polykondensation bilden können.
Wenn man nämlich von den phantasievollen Übertreibungen absieht, die von Nucleotiden oder gar von Polymeren wissen wollen, die bei MILLER-Versuchen entstanden sein sollen, So bleibt als Resultat des inzwischen an die hundertmal mit den verschiedensten Gasmischungen wiederholten MILLER-Versuchs (siehe Tab. S. 42): Neben relativ geringen Mengen von bifunktionellen Molekülen (wie Aminosäuren) enthalten Ursuppen ein Mehrfaches an monofunktionellen Molekülen. Die Hauptkomponenten: sind Ameisensäure und Methylamin, die als Salz (Methylammoniumformiat) die hydrolytische Aggressivität der Ursuppe bestimmen. Nucleotide, die Kettenbauteile von DNS oder RNS (auch Vorstufen derseIben), wurden bei MILLER-Versuchen mit Funkenentladungen nicht gefunden. Bei Versuchen mit Elektronenstrahlen (Höhenstrahlung, ß-Zerfall) wurde Adenin (eine von drei Komponenten des RNS/DNS-Kettenbestandteils Adenosinphosphat) in vierhundertfach geringerer Konzentration als Aminosäuren gefunden.1.0
Zahlenmäßig wird der beschriebene Einfluss eines Überschusses einer Art von funktionellen Gruppen und der Einfluss von Monofunktionellen * * auf die Kettenlänge durch folgende Gleichung beschrieben:
Abb. 22
PD = Polymerisationsgrad (Maß für die Kettenlänge)
q = nA : nB = Verhältnis der funktionellen Gruppen A und B * *
p = Umsatz = Anzahl der bei der Polykondensation umgesetzten Gruppen A oder B zu Anzahl der umsetzbaren Gruppen A + B
Abb. S. 58 zeigt die Abhängigkeit der Kettenlänge vom Verhältnis q gemäß GI. (2).
Man sieht, dass schon bei kleinsten Abweichungen von q = I die
Kettenlänge auf kleine Werte absinkt.
Der Überschuss an monofunktionellen Stoffen (Ameisensäure
Zum Einfluss des Gruppenverhältnisses q gemäß Abb. S. 56 auf die Kettenlänge (Pn)
q = I: gleich viele funktionelle Gruppen von beiden Sorten
Abb. 23
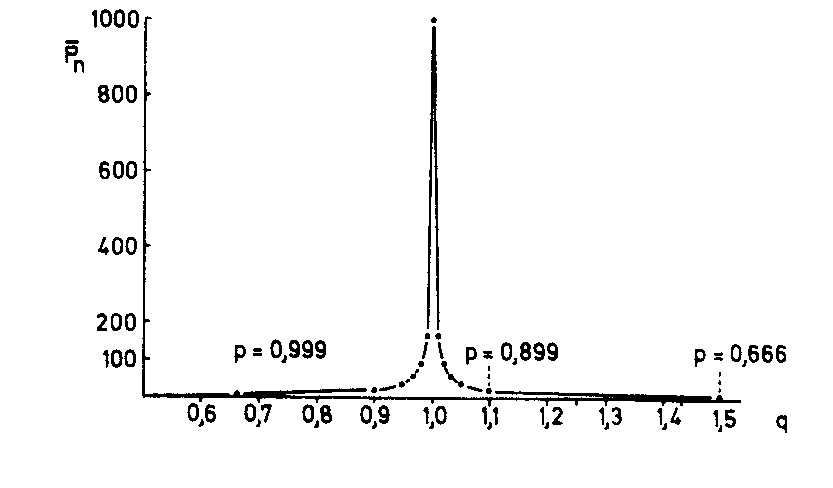
und Methylamin) ist im Hinblick auf die Frage nach der Proteinsynthese in Ursuppen So groß (q kleiner als 0,3) und im Hinblick auf die Frage nach der Möglichkeit einer Nucleinsäuresynthese so gewaltig (q kleiner als O,OOI), dass eine Polykondensation schon im Ansatz blockiert ist.
A.G. Cairns-Smith behandelt in seiner Arbeit Genetic takeover (1987; Cambridge University Press) u.a. die Unwahrscheinlichkeit der Entstehung von Nukleinsäuren in Ursuppen und erwähnt dazu folgende 19 Hauptpunkte (pp.56 59):
"The implausibility of prevital nucleic acid
If it is hard to imagine polypeptides or polysaccharides in primordial waters it is harder still to imagine polynucleotides. But so powerful has been the effect of Miller`s experiment on the scientific imagination that to read some of the literature on the origin of life (including many elementary texts) you might think that it had been well demonstrated that nucleotides were probable constituents of a primordial soup and hence that prevital nucleic acid replication was a plausible speculation based on the results of experiments. There have indeed been many interesting and detailed experiments in this area. But the importance of this work lies, to my mind, not in demonstrating how nucleotides could have formed on the primitive Earth, but in precisely the opposite: these experiments allow us to see, in much greater detail than would otherwise have been possible, just why prevital nucleic acids are highly implausible.
Let us consider some of the difficulties. First, as we have seen, it is not even clear that the primitive Earth would have generated and maintained organic molecules. All that we can say is that there might have been prevital organic chemistry going on, at least in special locations. Second, high-energy precursors of purines and pyrimidines had to be produced in a sufficiently concentrated form (for example at least 0.01 M HCN). Third, the conditions must now have been right for reactions to give perceptible yields of at least two bases that could pair with each other. Forth, these bases must then have been separated from the confusing jumble of similar molecules that would also have been made, and the solutions must have been sufficiently concentrated. Fifth, in some other location a formaldehyde concentration of above 0.01 M must have built up. Sixth, this accumulated formaldehyde had to oligomerise to sugars. Seventh, somehow the sugars must have been separated and resolved, so as to give a moderately good concentration of, for example, D-ribose. Eighth, bases and sugars must now have come together. Ninth, they must have been induced to react to make nucleosides. (There are no known ways of bringing about this thermodynamically uphill reaction in aqueous solution: purine nucleosides have been made by dry-phase synthesis, but not even this method has been successful for condensing pyrimidine bases and ribose to give nucleosides (Orgel & Lohrmann, 1974).) Tenth, whatever the mode of joining base and sugar it had to be between the correct nitrogen atom of the base and the correct carbon atom of the sugar. This junction will fix the pentose sugar as either the alpha or beta-anomer of either the furanose or pyranose forms (see page 29). For nucleic acids it has to be the beta-furanose. (In the dry-phase purine nucleoside syntheses referred to above, all four of these isomers were present with never more than 8 % of the correct structure.) Eleventh, phosphate must have been, or must now come to have been, present at reasonable concentrations. (The concentrations in the oceans would have been very low, so we must think about special situations -evaporating lagoons and such things (Ponnamperuma, 1978).) Twelfth, the phosphate must be activated in some way - for example as a linear or cyclic polyphosphate - so that (energetically uphill) phosphorylation of the nucleoside is possible. Thirteenth, to make standard nucleotides only the 5'hydroxyl of the ribose should be phosphorylated. (In solid-state reactions with urea and inorganic phosphates as a phosphorylating agent, this was the dominant species to begin with (Lohrmann & Orgel, 1971). Longer heating gave the nucleoside cyclic 2',3'-phosphate as the major product although various dinucleotide derivatives and nucleoside polyphosphates are also formed (Osterberg, Orgel & Lohrmann. 1973).) Fourteenth, if not already activated - for example as the cyclic 2',3'-phosphate - the nucleotides must now be activated (for example with polyphosphate; Lohrmann, 1976) and a reasonably pure solution of these species created of reasonable concentration. Alternatively, a suitable coupling agent must now have been fed into the system. Fifteenth, the activated nucleotides (or the nucleotides with coupling agent) must now have polymerised. Initially this must have happened without a pre-existing polynucleotide template (this has proved very difficult to simulate (Orgel & Lohrmann. 1974)); but more important, it must have come to take place on pre-existing polynucleotides if the key function of transmitting information to daughter molecules was to be achieved by abiotic means. This has proved difficult too. Orgel & Lohrmann give three main classes of problem. (i) While it has been shown that adenosine derivatives form stable helical structures with poly(U) - they are in fact triple helixes - and while this enhances the condensation of adenylic acid with either adenosine or another adenylic acid - mainly to di(A) stable helical structures were not formed when either poly (A) or poly(G) were used as templates. (ii) It was difficult to find a suitable means of making the internucleotide bonds. Specially designed water-soluble carbodiimides were used in the experiments described above, but the obvious pre-activated nucleotides -ATP or cyclic 2',3'-phosphates -were unsatisfactory. Nuc1eoside 5'-phosphorimidazolides, for example :
Abb. 24
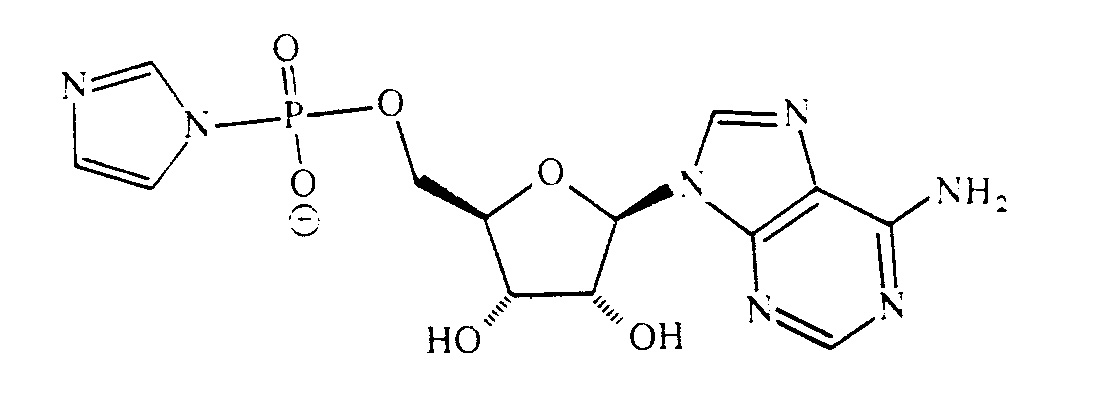
were more successful, but these now involve further steps and a supply of imidazole, for their synthesis (Lohrmann & Orgel, 1978). (iii) Internucleotide bonds formed on a template are usually a mixture of 2'-5' and the normal 3'-5' types. Often the 2'-5' bonds predominate although it has been found that Zn2+, as well as acting as an efficient catalyst for the template-directed oligomerisation of guanosine 5'-phosphorimidazolide also leads to a preference for the 3'-5' bonds (Lohrmann, Bridson & Orgel, 1980). Sixteenth, the physical and chemical environment must at all times have been suitable -for example the pH, the temperature, the M2+ concentrations. Seventeenth, all reactions must have taken place well out of the ultraviolet sunlight; that is, not only away from its direct, highly destructive effects on nucleic acid-like molecules, but away too from the radicals produced by the sunlight, and from the various longer lived reactive species produced by these radicals. Eighteenth, unlike polypeptides, where you can easily imagine functions for imprecisely made products (for capsules, ionexchange materials, etc.), a genetic material must work rather well to be any use at all - otherwise it will quickly let slip any information that it has managed to accumulate. Nineteenth, what is required here is not some wild one-off freak of an event: it is not true to say 'it only had to happen once'. A whole set-up had to be maintained for perhaps millions of years: a reliable means of production of activated nucleotides at the least.
Now you may say that there are alternative ways of building up nucleotides, and perhaps there was some geochemical way on the early Earth. But what we know of the experimental difficulties in nucleotide synthesis speaks strongly against any such supposition. However it is to be put together, a nucleotide is too complex and metastable a molecule for there to be any reason to expect an easy synthesis. You might want to argue about the nineteen problems that I chose: and I agree that there is a certain arbitrariness in the sequence of operations chosen. But if in the compounding of improbabilities nineteen is wrong as a number that would be mainly because it is much too small a number. If you were to consider in more detail a process such as the purification of an intermediate you would find many subsidiary operations -washings, pH changes and so on. (Remember Merrifield's machine: for one overall reaction, making one peptide bond, there were about 90 distinct operations required.)"
Diskussion weiterer Details wieder auf Wunsch. Ich meine jedoch, dass die oben aufgeführten Probleme, Gesetzmäßigkeiten und Tatsachen eindeutig belegen, dass Eigens Ausgangspunkt von einer Ursuppe, die so gehaltvoll war "wie eine kräftige Fleischbrühe" nicht den erdgeschichtlichen Realitäten entspricht. Wenn es darüber hinaus darum geht, Autoritäten ins Feld zu führen, dann darf ich mich auf den bekannten Nobelpreisträger Francis Crick berufen, der zum selben Ergebnis gekommen ist.
(Prof. C.:) "Angesichts der vielseitigen und anregenden Gedanken, die in dem Fachbereichs- und Fakultätsgrenzen überschreitenden Buch von Dr. Lönnig enthalten sind, würde ich mich über seine Habilitation durchaus freuen und die Meinung vertreten, dass seine Vorlesungen einen Gewinn für das geistige Leben jeder Universität darstellen würden. Voraussetzung dafür wäre allerdings angesichts der Forderung nach einem innovativen und dem letzten Stand der Wissenschaft entsprechenden Charakter von Habilitationsschriften, dass die in unseren Stellungnahmen enthaltenen Hinweise (und dazu noch weitere von anderer Seite) berücksichtigt und integriert werden. "
(W.-E.L.:)
(N.: Zunächst einmal ist dazu zu bemerken, dass ich rund sieben Jahre an der Univerrsität Bonn Seminare und Praktika zum großen Teil in eigener Verantwortung durchgeführt habe: Geschichte der Genetik, Humangenetik, Genetisches Praktikum für Mediziner. Und ich erinnere mich z.B. noch gut an einen Medizinstudenten, der mir nach der "Vorlesung" zum Thema Mitose und Meiose sagte, dass er das Thema schon oft gehört habe, aber noch nie in einer solch klaren und verständlichen Darstellung etc.. )Ich darf nun mit den hier vorliegenden Ausführungen in Anspruch nehmen, dass ich alle in Ihrer (N.: Herrn Prof. C.`s) Stellungnahme enthaltenen Hinweise unter Aufführung zahlreicher biologischer Tatsachen berücksichtigt habe (eine Diskussion von Herrn Prof. D.`s Kommentaren folgt, sobald mir das zeitlich möglich ist). Wie schon mehrfach betont, würde eine erschöpfende Diskussion der von Ihnen angeschnittenen Themenkreise noch weit umfassendere Erörterungen notwendig machen. Die hier aufgeführten Hauptpunkte zeigen meiner Auffassung nach jedoch bereits deutlich, dass die von mir befürworteten Thesen mit zahlreichen naturwissenschaftlichen Tatsachen begründet werden können. Weiter sollten die oben referierten Einwände zur Synthetischen Evolutionstheorie, insbesondere die neueren paläobotanischen Fakten und Interpretationen, in Vorlesungen und Lehrbüchern berücksichtigt werden.
Mit der Artbegriffsarbeit bin ich überdies nicht nur auf dem letzten Stand der Wissenschaft, sondern - (das klingt sicher etwas unbescheiden, und die Zukunft wird zeigen, ob das zutrifft) - in den Hauptpunkten der Zeit voraus.
(N.: Wie fast schon erwartet, kam von Herrn C. keine weitere Stellungnahme.)